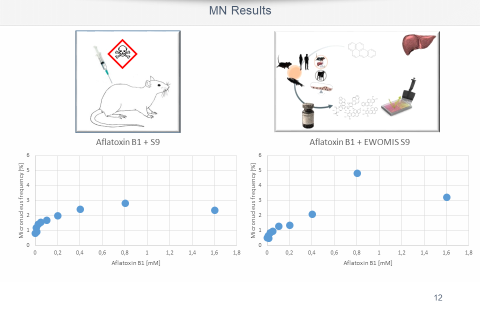
Der Mikrokerntest nach DIN EN ISO 21427-2 T5 2020-07 bzw . OECD No.487 ist ein in vitro Verfahren, das eine Schädigung des Erbgutes und damit eine krebsauslösende Veränderung der Zelle erfasst. Bisher beschränkte sich das Verfahren darauf, den Biomarker „Mikrokern“, eine chromatinhaltige Struktur, die zusätzlich zum Hauptkern auftritt, in Kulturen von Säugerzellen als eine Folge der Exposition gegenüber einer Prüfsubstanz zu dokumentieren. Mikrokerne/Kleinkerne wurden bislang mittels Chromatinfärbetechniken an fixierten Zellen nachgewiesen.
GOBIO hat eine innovative Variante des Verfahrens als akkreditierte Hausmethode HM 21427-2 entwickelt, bei der Mikrokerne an lebenden Zellen mittels Lebendbildanalyse erfasst werden können. Das Verfahren basiert auf einer gesunden Zelllinie, die ein Histon 2B Grünfluoreszenz-Fusionsprotein expremiert. Dadurch sind Chromatinstrukturen wie Mikrokerne mittels Fluoreszenzmikroskopie in der lebenden Zelle sichtbar. Die Zellen die GOBIO für den Mikrokerntest einsetzt, sind weder von Tumoren abgeleitet noch anderweitig immortalisiert. Sie verfügen über eine natürliche Kontrolle des Zellzyklus und sind metabolisch kompetent.
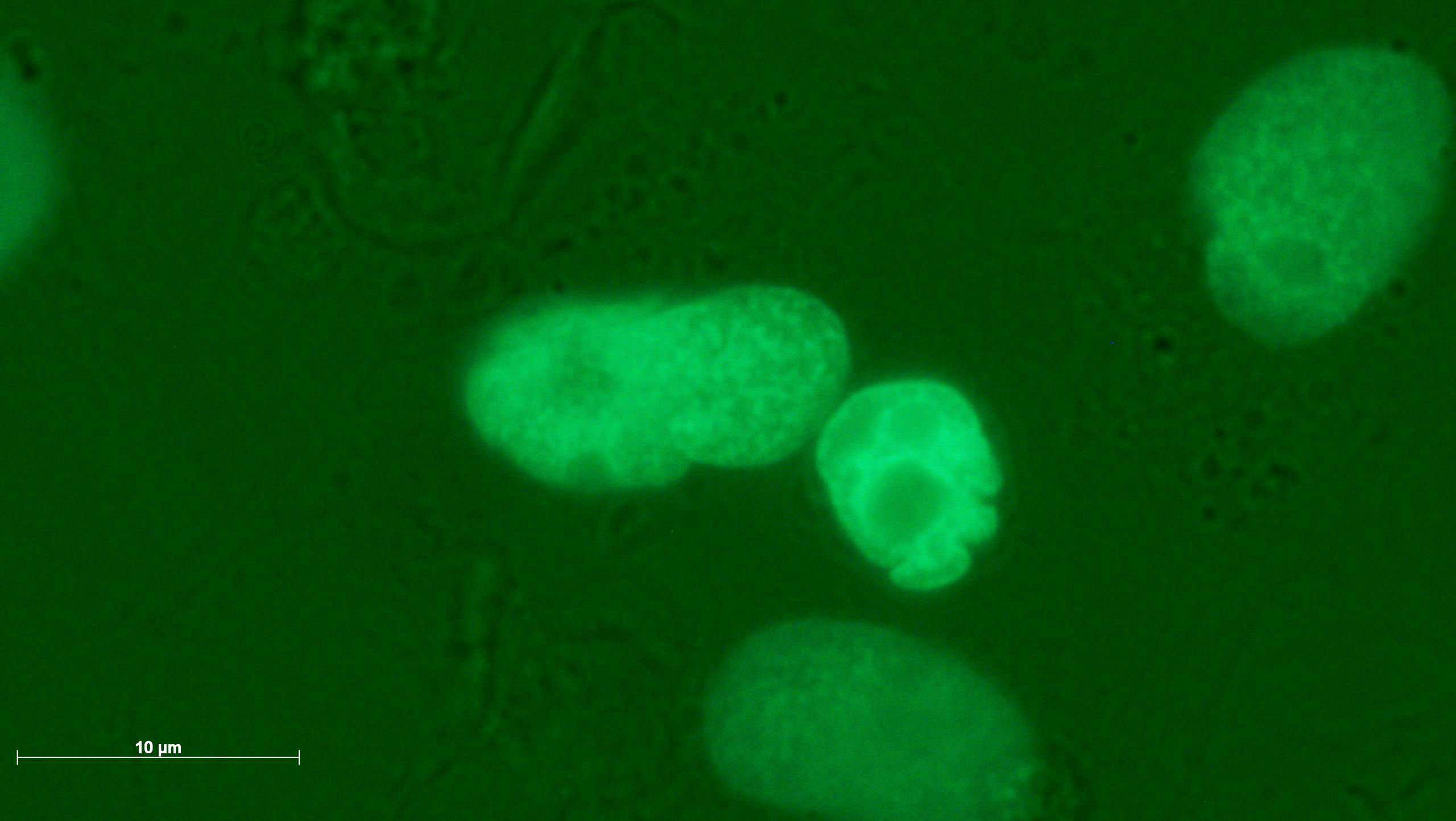
Sie sind zu natürlichem Zelltod fähig. Aufgrund dieser Eigenschaften kann über den Biomarker „Mikrokern „ hinaus auch eine Transformation der vormals gesunden Zelle zur Krebszelle geprüft werden. Folgende Veränderungen der Kernmorphologie treten auf wenn eine maligne Transformation stattfindet.
Testdurchführung
In der Regel wird zunächst ein Rangefinder-Test zur Bestimmung der Zytotoxizität durchgeführt. Der Test wird auf 96 well-Platten durchgeführt. Die Schadstoffexposition erfolgt in 4 subzytotoxischen Konzentrationen (8 wells pro Konzentration) wenn die adhärent wachsenden Zellen eine Konfluenz von 60 % erreicht haben. Es werden Positiv- und Negativkontrollen in jedem Experiment mitgeführt. Die Mikrokernfrequenz in Testansätzen wird anhand von 2 automatisiert erstellten Bildern/pro well software gestützt ermittelt. Zur Identifizierung von Micronuclei wird sowohl das Fluoreszenzbild als auch die Überlagerung mit der Hellfeldaufnahme analysiert.
Auf Kundenwunsch kann die Messung zu verschiedenen Zeitpunkten durchgeführt werden. Dies ermöglicht das Erkennen von reversiblen Effekten, z.B. die Wiedereingliederung von Mikrokernen während der Interphase.
Bitte hinterlassen Sie Ihre Kontaktdaten, wenn Sie weitere Informationen wünschen. Link zum Kontaktformular.
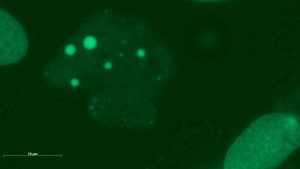
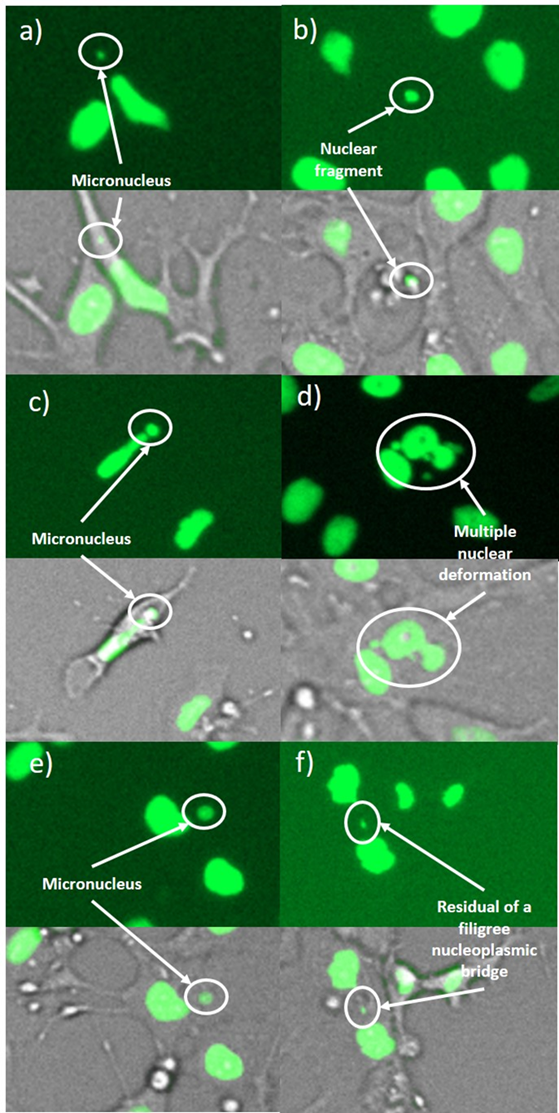
Genotoxisches Schädigungsmuster mit (a,b) Mikronuklei, (c) einem großen Mikronukleus, (d) einem mehrfach deformierten Kern, (e) einem Kernfragment außerhalb einer Zelle und (f) einem Rest einer filigranen nukleoplasmatischen Brücke. Die Bilder wurden in 4-NQO-exponierten Kulturen (a,b,d), in Colchicin-exponierten Kulturen (c,e) und in Cannabidiol-exponierten Kulturen (f) aufgenommen.
Die Vorteile des neuen, kostengünstigen Mikrokerntests
Hölzel, B.N., Pfannkuche, K., Allner, B. et al. Following the adverse outcome pathway from micronucleus to cancer using H2B-eGFP transgenic healthy stem cells. Arch Toxicol 94, 3265–3280 (2020). Zur Veröffentlichung.
- Leistungsmerkmale gemäß DAkkS-geprüfter SOP:
Erkennung von zytogenetischen Schädigungen an nicht immortalisierten, gesunden Zellen mit funktioneller Proliferationskontrolle.
- Die Methode stimmt in den Grundfunktionen mit OECD Guideline Nr. 487/ DIN EN ISO 21427-2 T5 überein, also der Erfassung von vornehmlich mitotisch entstandenen zytogenetischen Schäden. Da die Kultur anders als synchronteilende immortalisierte Zellen auch langlebige Stammzellen umfasst, werden auch Schäden, die während der Interphase entstehen, zuverlässig erfasst.
- Die Methode ist Wirkmechanismus-basiert. Es werden auch Submechanismen abgebildet
- Damit geht der Test über die Merkmale von OECD Guideline Nr. 487/ DIN EN ISO 21427-2 T5 hinaus
- Aufgrund der Vielzahl an zellulären Funktionen, die in der H2B-GFP-KCB Zelllinie beobachtet werden können, sind nicht-dosisbezogene Effekte denkbar, z.B. Eingriffe in die genetische Grundlage von Motilität.
- Deshalb wird das Kriterium der Dosisabhängigkeit berichtet, es ist aber kein Ausschlusskriterium für die Beurteilung der Gentoxizität.
- Zeitnahe Ergebnisse: 14 Tage nach Bereitstellung der Prüfsubstanz/des Testgutes
- GLP-konformer Prüfbericht
- Umfangreiche elektronische, exposé-fähige Dokumentation der Auswertung der Bilddateien
- Cytotoxizitätsprüfung enthalten ohne Zusatzkosten
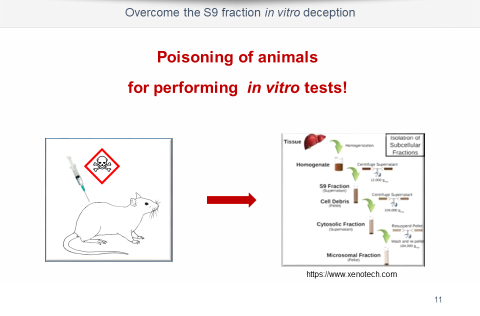
- Tierversuchsfreie, metabolische Aktivierung der Testsubstanz
- Reversibilität kann durch Messung zu verschiedenen Zeitpunkten erkannt werden
- Weitere Parameter des Gesundheitszustandes der Zellen kostengünstig abrufbar z.b. Mitoseindex, Motilität. Downstream Analysen möglich: Cytokinese-/Interphasedauer, Apoptose Pyknotisierung, Genexpressionsanalysen auf der Grundlage eines bekannten Expressoms.